Ile m3 dwutlenku węgla zostanie wyemitowane do atmosfery po spalenia 1 m3 gazu?
Nie masz pojęcia, nie wiesz nawet, gdzie i jak możesz takie dane znaleźć?
– No, to poszukaj odpowiedzi w swoich podręcznikach chemii (no i oczywiście w Google u, który wszystko wie)!
Jeżeli jednak mimo usilnych starań i szczerej chęci nie znajdziesz odpowiedzi na to bardzo ważne dla wszystkich pytanie, to najprościej będzie, jeżeli rozwiążesz to zadanie sam. Wbrew pozorom nie jest ono wcale trudne.
No, dobrze, ale po co w ogóle mam rozwiązywać to zadanie?! I to pytanie jest też bardzo dobre! – Po co?
Dwutlenek węgla jest złym przewodnikiem ciepła. Nawet bardzo niewielki wzrost jego stężenia w atmosferze powoduje tzw. efekt cieplarniany.
Coraz większa część ciepła, które ziemia otrzymuje ze słońca, zamiast zostać wypromieniowana przez ziemię w przestrzeń kosmiczną jest zatrzymywane przez znajdujący się w atmosferze dwutlenek węgla i pozostaje na ziemi.
Na skutek tego temperatura atmosfery ziemskiej, bardzo powoli, ale ciągle wzrasta. W konsekwencji lodowce topnieją, poziom wód w morzach i oceanach zaczyna się podnosić i coraz częściej pojawiają huragany, powodzie, susze oraz różnego rodzaju anomalie pogodowe.
Wiesz już teraz, dlaczego należy rozwiąż ac to zadanie. Rozwiązanie tego zadania wymaga zaznajomienia się z podstawowymi własnościami gazów zebranymi w poniższej tablicy .
Podstawowe własności niektórych gazów (tablica 1)
Mol
Nazwa Wzór Objętość, dcm Masa, g
Metan CH4 22,414 16
Tlen O2 22,414 32
Dwutlenek węgla CO2 22,414 44
Tlenek węgla CO 22,414 28
Para wodna H2O 22,414 18
Azot N2 22,414 28
Wodór H2 22,414 2
Hel He 22,414 4
Butan C4H10 22,414 58
Przyglądnij się uważnie zebranym w tablicy danym i podsumuj w myśli, co wiesz o tych gazach
Metan jest głównym i dominującym składnikiem gazu ziemnego, na którym Twoja mama przygotowuje różnego rodzaju pyszności.
Gaz ten rozprowadzany jest rurociągami między państwami, miastami oraz poszczególnymi domami. Jest też transpirowany statkami w postaci skroplonej. Zamiast nazywać go gazem ziemnym lub naturalnym lepiej byłoby nazywać go metanem. Ta poprawna chemicznie nazwa uczulałaby użytkowników, że nie jest gaz tak samo bezpieczny jak powietrze i wymaga przestrzegani podstawowych zasad bezpieczeństwa: po otwarciu kurka należy go zapalić, a po zamknięciu gazu sprawdzić, czy kurek jest zamknięty i gaz się nie ulatnia
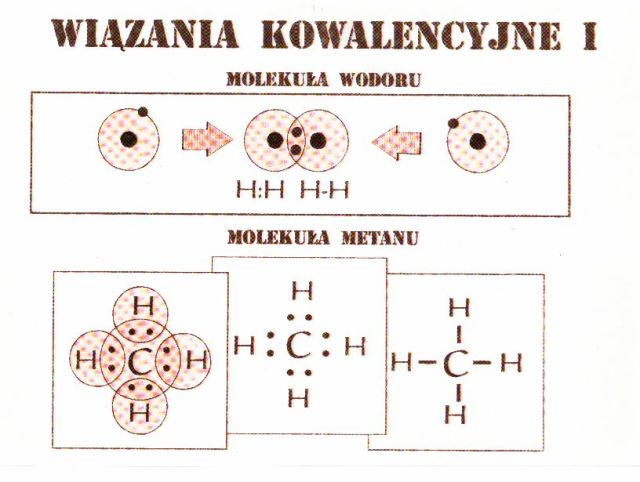
Cząsteczka metan CH4 zbudowana jest z jednego atomu węgla C oraz z czterech atomów wodoru H, na co wskazuje dolny indeks 4. Przy symbolu atomu węgla C powinien być wpisany dolny indeks 1. Dla wygody nie piszemy indeksu 1, ale nie należy jednak zapominać o tej pominiętej jedynce, bo ona tam jest.
Symbol C może oznaczać nie tylko pojedynczy atom węgla, ale i nazwę pierwiastka węgla. Kaidy pierwiastek składa się z jednego tylko rodzaju atomów. W tym przypadku może to być zarówno grafit, jak i diament.
Symbol Au może oznaczać zarówno jeden atom złota, jak i samorodek złota składający się z samych tylko atomów złota. Podobnie Cu może reprezentować jeden atom miedzi, jak i pierwiastek, z którego wykonano miedziany drut lub blachę.
Tlen O z węglem C i wodorem H można nazywać pierwiastkami życia. Nie ma na świecie żywego organizmu, który nie byłby zbudowany z tych trzech pierwiastków.
Powietrze jest mieszaniną tlenu O2 w 21 % oraz z 79 % z azotu N2. Zarówno tlen, jak i azot nie występują w powietrzu w postaci pojedynczych atomów, tylko w postaci dwuatomowych cząsteczek tlenu O2 i azotu N2. Azot z powietrza wykorzystuje się w do produkcji nawozów azotowych.
Hel i inne gazy szlachetne występują w powietrzu w śladowych ilościach jako pojedyncze atomy, a nie w postaci dwuatomowych cząsteczek. Hel i wodór w przeciwieństwie do dwutlenku węgla są dobrymi przewodnikami ciepła. Trudno będzie Ci uwierzyć, że hel został odkryty najpierw na słońcu, a dopiero potem na ziemi!
Dwutlenek węgla jest głównym produktem spalania nie tylko nie tylko metanu, ale i wszystkich paliw ciekłych (ropopochodnych), jak również paliw stałych takich jak węgiel kamienny, węgiel brunatny, drewno, torf, koks itp.
Aby przystąpić do rozwiązania postawionego na wstępie zadania powinieneś jeszcze uporządkować swoje wiadomości o reakcjach chemicznych i równaniach chemicznych,.
Równanie reakcji spalania metanu
Każde równanie chemiczne jest ilościowym opisem jakiejś reakcji chemicznej. Jest też równaniem w sensie matematycznym: zarówno lewa, jak i prawa strona równania chemicznego muszą być sobie równe.
W przypadku reakcji spalania metanu metan reaguje z tlenem znajdującym się w powietrzu, a w wyniku tej reakcji powstają dwie nowe substancje: dwutlenek węgla oraz woda w postaci pary wodnej.
CH4 + O2 = CO2 + H2O (1)
Po lewej stronie znaku równości zapisujemy wzory sumaryczne substratów, czyli tych substancji, które reagują z sobą, a po prawej stronie wzory sumaryczne produktów reakcji, czyli tych substancji, które powstają w wyniku reakcji chemicznej.
Substratami reakcji spalania metanu są: metan i tlen, a produktami reakcji są dwutlenek węgla oraz para wodna.
Coś się nie zgadza w tym zapisie równania 1?
Istotnie, liczby atomów tlenu i wodoru po obu stronach równania nie są sobie równe! Trzeba równanie zbilansować w taki sposób, aby liczby atomów po lewej i po prawej stronie równania chemicznego były sobie równe zgodnie z prawem zachowania masy. Bilansowanie równań reakcji chemicznych nie jest wcale takie trudne, jak to się może wydawać.
W powyższym równaniu (a raczej w nierówności) atomów tlenu wystarcza tylko na utworzenie dwutlenku węgla, ale zabrakło go na utworzenie dwóch cząsteczek wody z obecnych w cząsteczce metanu czterech atomów wodoru.
Wprowadzamy odpowiednie korekcje i otrzymujemy poprawnie zbilansowane równanie reakcji spalania metanu.
CH4 + 2O2 = CO2 + 2H2O (2)
Na podstawie poprawnie zbilansowanego równania reakcji spalania metanu można powiedzieć, że jedna cząsteczka metanu reaguje z dwoma cząsteczkami tlenu. W wyniku tej reakcji powstaje jedna cząsteczka dwutlenku węgla oraz dwie cząsteczki wody (pary wodnej).
Porównaj jeszcze raz oba te oba te zapisy reakcji chemicznej i sprawdź, czy po obu stronach równania zbilansowanego masz taką samą liczbę atomów każdego z pierwiastków.
Gazy podane w tablicy 1 składają się z ciasteczek związków chemicznych, na przykład metanu CH4 , dwutlenku węgla CO2 i wody H2O .
Cząsteczki związków chemicznych składają się z atomów różnych pierwiastków.
Cząsteczki gazów mogą być też zbudowane z atomów jednego rodzaju atomów, na przykład tlenu O2, i ozonu O3 azotu N2 itd.
Hel i inne gazy szlachetne nie tworzą cząsteczek i składają się z pojedynczych atomów każdego z tych pierwiastków.
Objętość jednego mola gazu jest taka sama, wynosi 22 (lub dokładnie 22,414 dcm) i nie zależy od rodzaju gazu (tablica 1). W objętości molowej każdego gazu znajduje się taka sama liczba cząsteczek gazu. Jest to niewyobrażalnie duża liczba nazywana liczbą Avogadra.
Liczba Avogadra jest liczbą atomów w 12 g izotopu węgla 12C. Liczba Avogadra jest liczbą wzorcową, na której opiera się cała buchalteria chemiczna.
W 22 dcm znajduje się tyle samo ciasteczek helu co i dwutlenku węgla. Nie należy jednak zapominać, że przy takiej samej objętości molowej masa jednego mola helu wynosi zaledwie 4 g (lekki gaz), a masa jednego mola dwutlenku węgla aż 44 g (ciężki gaz). Mimo tej różnicy w 4 g helu znajduje się tyle samo atomów co i cząsteczek w 44 g dwutlenku węgla.
Równanie nie ulega zmianie, jeżeli obie jego strony zostaną pomnożone przez ta samą liczbę, na przykład liczbę Avogadra LA.
1*LA CH4 + 2**LA O2 = 1**LA CO2 + 2**LA H2O (3)
Z zapisu tego wynika, że 1 mol metanu reaguje z dwoma molami tlenu w wyniku czego powstaje jeden mol dwutlenku wegna oraz dwa mole wody.
CH4 + 2O2 = CO2 + 2H2O
Współczynniki w powyższym równaniu mogą oznaczać liczby uczestniczących w reakcji cząsteczek reagentów lub liczbę moli tych reagentów (obliczenia stechiometryczne).
Masz teraz wystarczająco dużo wiadomości, aby samodzielnie rozwiązać postawione na wstępie zadanie Swoje rozwiązanie opublikuj w formie komentarza do tego wpisu (c. d. n. lub nie!)!